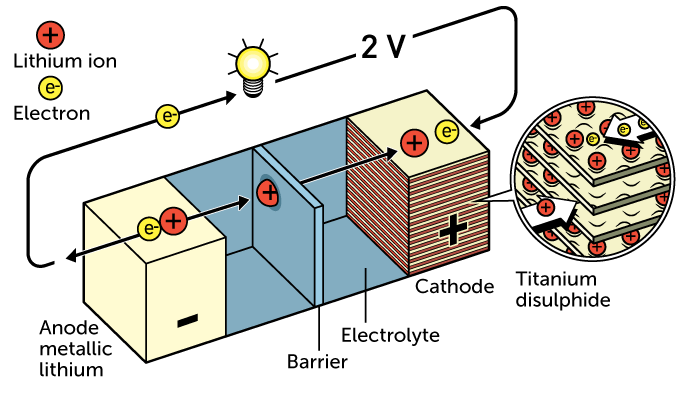
La creación de un mundo recargable le ha valido a tres científicos el Premio Nobel de Química 2019. John B. Goodenough de la Universidad de Texas en Austin, M. Stanley Whittingham de la Universidad Binghamton en Nueva York y Akira Yoshino de la Corporación Asahi Kasei en Tokio y la Universidad Meijo en Nagoya, Japón, ganaron por sus contribuciones al desarrollo de baterías de iones de litio . Estas baterías livianas y recargables alimentan todo, desde dispositivos electrónicos portátiles hasta autos eléctricos y bicicletas, y proporcionan una forma de almacenar energía de fuentes de energía renovables pero transitorias, como la luz solar y el viento. "Esta batería ha tenido un impacto dramático en nuestra sociedad", dijo Olof Ramström, químico de la Universidad de Massachusetts Lowell y miembro del Comité Nobel de Química de 2019, el 9 de octubre durante el anuncio del premio por la Real Academia de Ciencias de Suecia. en Estocolmo “Está claro que los descubrimientos de nuestros tres galardonados realmente hicieron esto posible. Realmente ha sido para el mejor beneficio de la humanidad ". Estos laureados recientemente acuñados compartirán igualmente el premio de 9 millones de coronas suecas (alrededor de $ 900,000). Goodenough, de 97 años, es la persona más vieja en recibir un Premio Nobel. "John es un científico increíble, con una intuición increíble, y una gran persona, que ha inspirado a generaciones de científicos e ingenieros con su actitud positiva, honestidad y curiosidad ilimitada", dice Yang Shao-Horn, químico e ingeniero del MIT. Las baterías almacenan energía eléctrica en forma de energía química y tienen tres partes principales: dos electrodos (el ánodo o electrodo negativo y el cátodo, positivo) y el electrolito, que ayuda a los iones a moverse dentro de la batería. Las reacciones químicas en un extremo de la batería, en el ánodo, liberan electrones que viajan a través de un circuito al otro extremo y son aceptados por el cátodo, formando una corriente que puede alimentar una linterna, un teléfono celular o un automóvil. Estos laureados recientemente acuñados compartirán igualmente el premio de 9 millones de coronas suecas (alrededor de $ 900,000). Goodenough, de 97 años, es la persona más vieja en recibir un Premio Nobel. "John es un científico increíble, con una intuición increíble, y una gran persona, que ha inspirado a generaciones de científicos e ingenieros con su actitud positiva, honestidad y curiosidad ilimitada", dice Yang Shao-Horn, químico e ingeniero del MIT. Las baterías almacenan energía eléctrica en forma de energía química y tienen tres partes principales: dos electrodos (el ánodo o electrodo negativo y el cátodo, positivo) y el electrolito, que ayuda a los iones a moverse dentro de la batería. Las reacciones químicas en un extremo de la batería, en el ánodo, liberan electrones que viajan a través de un circuito al otro extremo y son aceptados por el cátodo, formando una corriente que puede alimentar una linterna, un teléfono celular o un automóvil. Alessandro Volta demostró la primera batería eléctrica en 1800, y los científicos han estado clamando por construir mejores baterías desde entonces, principalmente buscando materiales anódicos que puedan liberar más electrones y materiales catódicos que puedan atraerlos mejor. En la década de 1970, Whittingham comenzó a experimentar con el litio como material anódico, porque es muy liviano y libera electrones e iones de litio cargados positivamente. Su esquema de batería recargable utilizaba un cátodo hecho de disulfuro de titanio, que contiene muchas capas que pueden alojar iones de litio liberados del ánodo. Mientras trabajaba con la compañía energética Exxon, Whittingham combinó metal de litio y disulfuro de titanio en una batería, creando la primera batería de litio. Su batería contaba con 2 voltios. Pero el metal de litio que comprendía el ánodo original de Whittingham podría formar defectos llamados dendritas ( SN: 26/10/17 ) que podrían causar un cortocircuito y una explosión de la batería. Por lo tanto, los desarrolladores agregaron aluminio al ánodo de litio y cambiaron la sustancia electrolítica intercalada entre el ánodo y el cátodo para hacer una batería más segura para el uso diario. Luego, a fines de la década de 1970 y principios de la década de 1980, Goodenough buscó mejorar el cátodo de Whittingham utilizando en su lugar óxido de cobalto. Este material estaba en capas como el disulfuro de titanio, pero podía albergar aún más iones dentro de sus capas. La innovación de Goodenough duplicó el potencial de voltaje de las baterías de litio a 4 voltios, "un salto gigantesco en el mundo de las baterías", dijo Ramström durante la conferencia de prensa. (Muchos teléfonos inteligentes actuales usan baterías de litio con voltajes de alrededor de 4 voltios). Pero la batería todavía usaba litio metálico como ánodo...

Comentarios